探索研究から商業化までを包括的に支える AAV 試験サービス
アデノ随伴ウイルス(AAV)は、長期にわたる遺伝子発現、非病原性、そして極めて低い免疫原性といった、遺伝子導入における大きな利点を備えています。
一方で、AAV の製造には依然として多くの課題があります。規制要件は複雑かつ絶えず変化しており、また血清型を問わず凝集が発生することがあります。さらに、製造された製品には、完全なカプシド、空のカプシド、部分的に充填されたカプシドが混在する可能性があります。加えて、AAV は非複製性であるため、プロセスおよび製品の特性解析は非常に困難です。
ザルトリウスは、研究開発段階から規制当局による承認取得までを幅広く支援する AAV 試験サービスを提供しています。確保された試験枠と、経験豊富な専任チームによる専門性を活かし、AAV 製造のあらゆるフェーズを力強くサポートします。
AAVの特性解析手法
規制要件への対応をスムーズに
規制環境は複雑で、日々変化しています。規制当局は新たな AAV ガイダンスを継続的に発行しており、わずかな手違いでも承認プロセスが長期化し、コスト増を招く可能性があります。
ザルトリウスは、安全性、同一性、純度、有効性といった重要指標にもとづく AAV 特性解析について、開発から確立、バリデーションまで一貫して支援します。ザルトリウスのチームは、FDA や EMA/CAT における承認取得支援の実績に加え、韓国・日本・中国のガイドラインに関する深い知識も有しており、グローバル規制への対応を力強くサポートします。
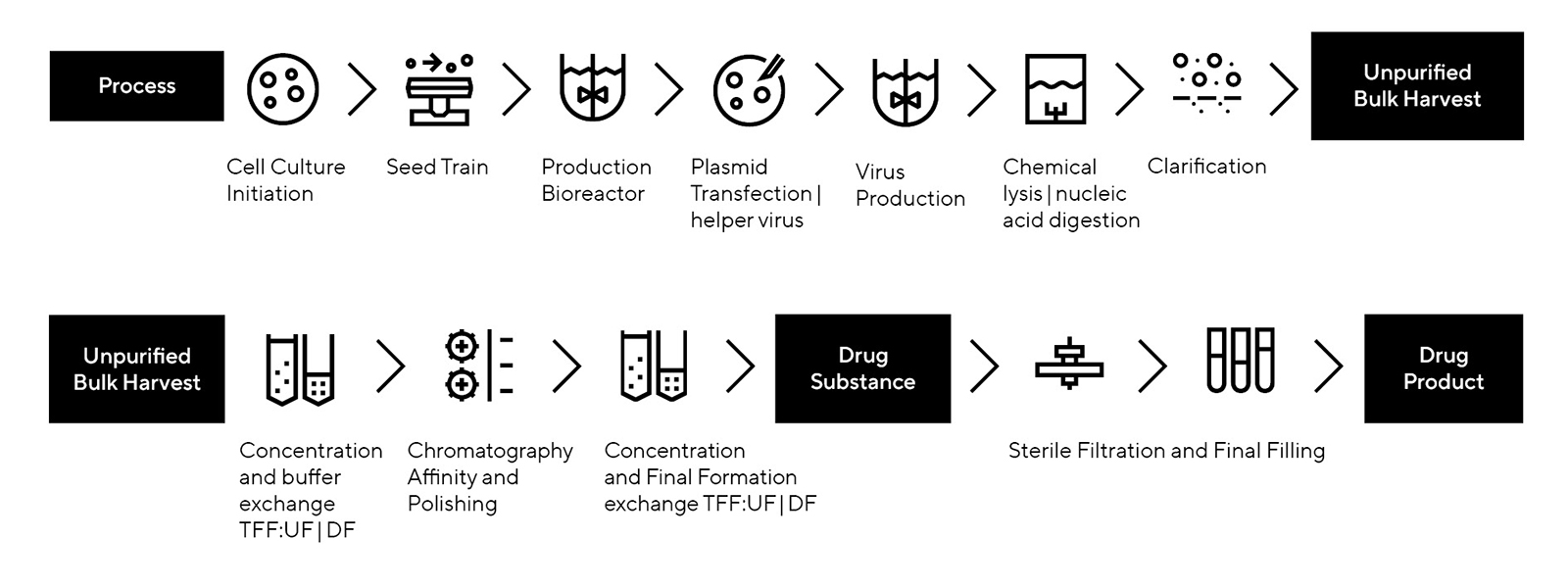
以下の属性をテストする方法
製品の固有の同一性を確認し、製品またはプロセスの他の構成要素と区別します。
カプシドの同一性
目的遺伝子
全ゲノム配列
完成品中の不純物が最小限に抑えられていることを示します。
- 全量:空カプシド比
- 残留物HCP、DNA、BSA、ベンゾナーゼ、リガンド、およびプラスミド
- トランスフェクション剤および界面活性剤
- 残留物トランスフェクション試薬 (FectoVIR®-AAV および PEIpro®に対する特定の方法を含む )
- 凝集
医薬品の治療効果を定義します。
感染性
ゲノム滴度
ウイルス異物力価
製品がウイルスや微生物などの外来物質を含まないことを確認します。
- 無菌性およびマイコプラズマ
- エンドトキシン
- 外来ウイルス
- 複製能:rcAAV
- 種特異性ウイルス
初期開発段階における製品特性解析の効率化
初期開発段階では、試験方法を外部に委託することで、基本的な製品特性評価にかかる時間を短縮できます。ザルトリウスの最適なソリューション選定と専門知識により、プロセス開発に集中でき、最終的な収率を高めるとともに、次の開発段階へより早く進むことが可能になります。
初期段階から臨床試験への移行を円滑に進める
AAV 医薬品候補が前臨床試験に進む準備が整ったと判断された段階では、製造メーカーは製品およびプロセスに由来する不純物を評価し、包括的な特性解析を実施する必要があります。
ザルトリウスでは、一般的な製品品質や物理化学的特性を含む幅広い特性解析により、AAV 製品の臨床試験への移行を支援します。また、試験方法は、規制要件の順守とアッセイの汎用的な適格性確認をサポートするよう設計されています。
後期開発および商業化プロセスを加速
後期臨床試験への移行や商業化を進めるためには、規制要件を満たす完全な製品特性解析に加え、対象となる AAV 製品および開発段階に適合したバリデーション済みの試験法が必要です。
ザルトリウスの事前適格性評価済みの試験方法や、すぐに利用可能な off‑the‑shelf アッセイを活用することで、迅速なターンアラウンドを実現できます。製品固有の最適化が必要な場合でも、ザルトリウスのチームは最も広く使用されている AAV 血清型向けにアッセイを開発し、適格性確認を行っています。
試験方法|規制ガイドライン
以下の表は、規制ガイドラインで義務付けられている試験方法の概要と、各開発段階で実施すべき試験内容を示しています。
ザルトリウスの製品ポートフォリオ
遺伝子細胞治療を支えるザルトリウスのソリューション
ザルトリウスは、人々の人生を変える遺伝子・細胞治療を実現するという使命をお客様と共有しています。再現性の高い性能とスケーラビリティを両立するエンドツーエンドのソリューションにより、規制当局の承認取得プロセスを簡素化し、商業化までの道のりを加速させます。
よくあるご質問 - AAVサービス
はい。ザルトリウスでは、臨床および商業段階での規制要件への対応を支援する GMP 準拠の試験方法 に加え、前臨床段階に適した 非 GMP 試験方法も提供しています。
ザルトリウスの AAV 試験は、 FDA および EMA/CAT のガイダンスに加え、韓国、日本、中国の規制当局によるガイダンスにも準拠しています。
2020 年 1 月、FDA は 「ヒト遺伝子治療治験薬申請における化学・製造・管理(CMC)情報に関する業界向けガイダンス」(FDA CBER, January 2020) を発行しました。一方、欧州では依然として 「遺伝子治療医薬品の品質、非臨床および臨床的側面に関するガイドライン」(EMA/CAT/80183/2014) が適用されています。
これらのガイダンスでは、すべての医薬品について 安全性、同一性、純度、有効性 が保証されていることが求められています。
はい、提供しています。こちらのページに掲載されていない試験法にご関心がある場は、お気軽にお問い合わせください。ザルトリウスはこれまで 15 年以上にわたり、お客様向けに試験法の開発および提供を行ってきました。
その他のウイルスベクターに対する試験についても、まずはお問い合わせください。お客様のご要望に応じて詳細をご相談させていただきます。
既存の試験サービスおよびセルバンキングサービスに加え、AAV 試験専用の試験枠をご用意しています。ザルトリウスではグローバルにサービスを提供しており、リードタイムについては毎週最新情報を更新しています。