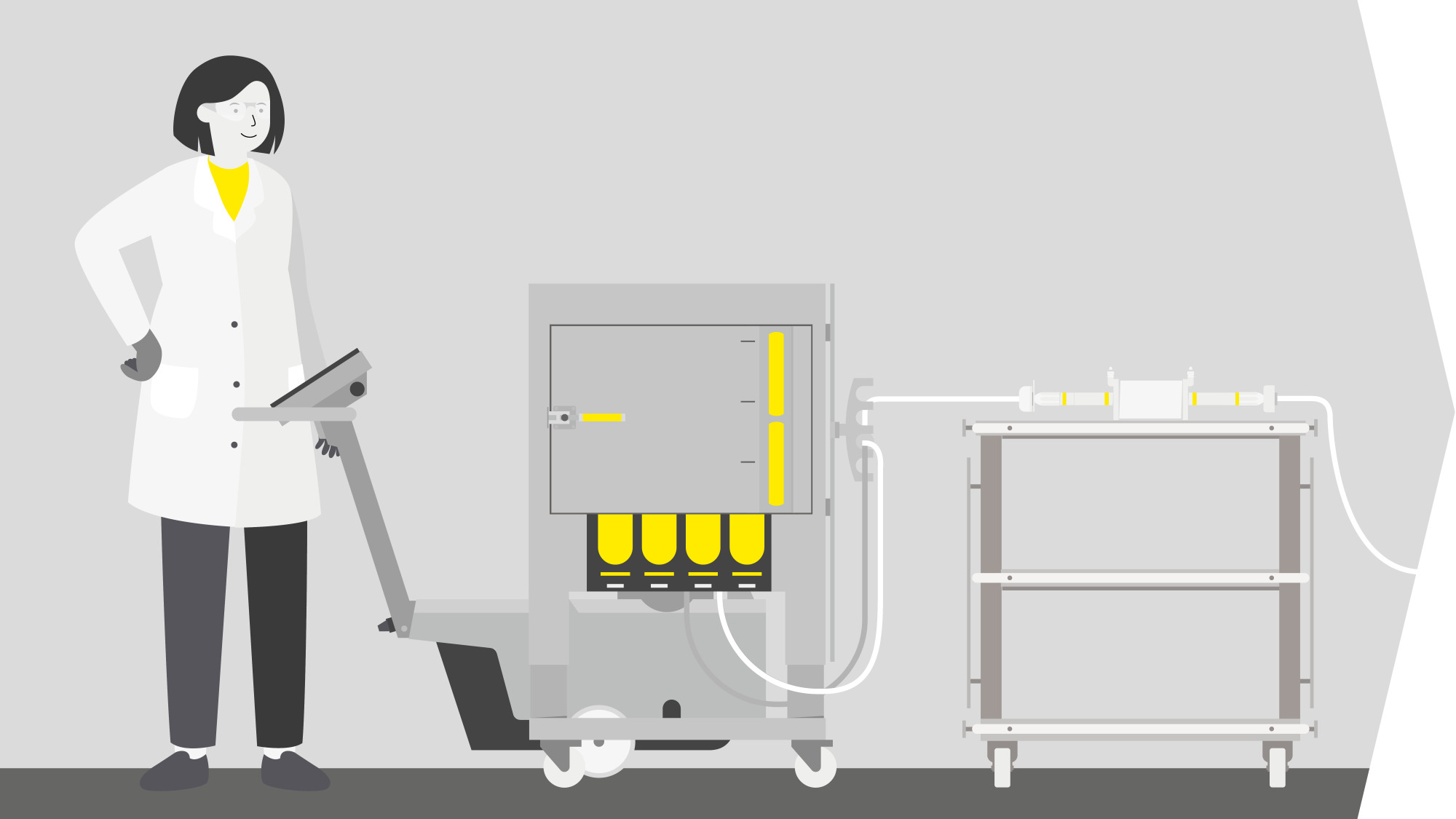
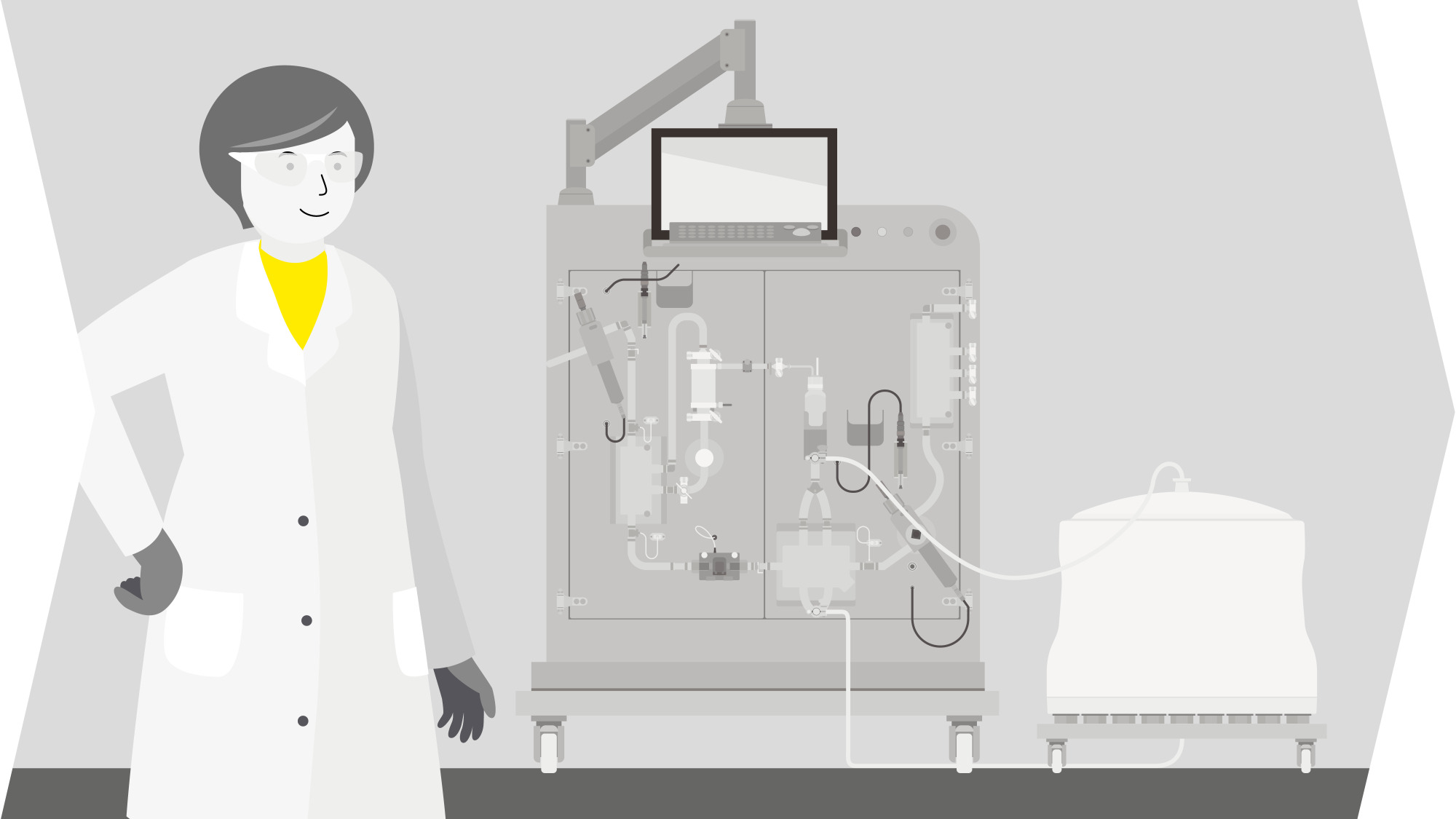
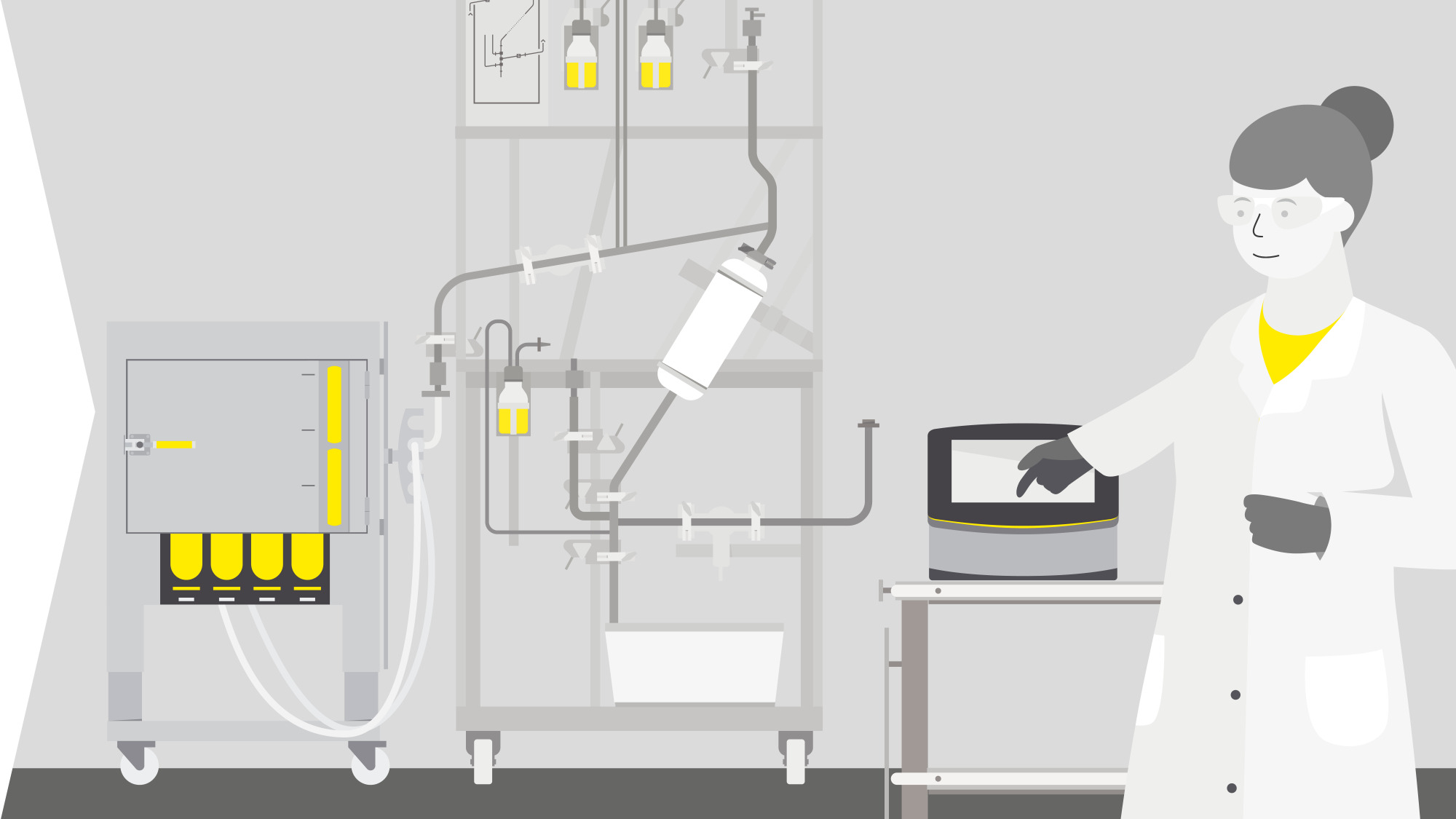
AAV遺伝子治療のワークフロー
AAVワークフローのためのソリューション
サンプルの要望 | 原料および消耗品
お客様のニーズに合った適切な材料や消耗品をお探しいただくため、当社のポートフォリオからサンプルをご請求ください。
よくあるご質問 - AAV遺伝子治療
AAVは直径30ナノメートル未満の小型ウイルスであり、主にエピソーム発現を示すカプシド内に5キロベースのDNAを含みます。カプシドタンパク質の発現状態によって異なる血清型が存在し、臓器特異的な標的化をサポートします。通常、HEK293細胞への2~3種類のプラスミドのトランスフェクションにより生産され、その後ろ過およびクロマトグラフィーによる精製を経て不純物が除去されます。
重要品質特性(CQAs)は通常、リスク評価の過程で設定され、開発中の特定の医薬品によって異なります。ほとんどの医薬品では、製品の安全性、アイデンティティー、無菌性、純度、および有効性に重点が置かれます。アデノ随伴ウイルス(AAV)療法の場合、有効性の測定は困難を伴います。有効性評価には、ゲノム量やカプシド量の測定、ならびにトランスデューション効率の評価が含まれる場合があります。副作用を回避するためには純度の確保も極めて重要であり、したがって、空のAAV異物、DNA、タンパク質含有量などの不純物のモニターが不可欠です。
AAVプロセスの性能向上に向け、HEK細胞培地ならびにFectoVIR®-AAVやpPLUS® AAV-Helperなどのトランスフェクション試薬をご提供しております。250mLから2000Lまで同一構造のシングルユースバイオリアクターと組み合わせることで、スケールアップの簡素化を実現いたします。
また、清澄化ソリューションとして、Sartoclear®デプスフィルター、Hydrosart®フィルターカセット、Sartopore® 2 XLG滅菌フィルター、モノリスカラムなど、プロセス開発から大規模製造までスケーラブルなソリューションを、シングルユースおよび閉鎖系フォーマットでご提供しております。
ダウンストリームプロセスでは、医薬品の安全性と有効性を最大化するため、DNAやHCPなどの不純物を除去する必要があります。AAV製造においては、大量の空のカプシド(最大80%)を分離することが課題となります。これは、それらが完全なカプシドと類似しているためです。また、AAVの濃縮過程では、フィルター材料への結合による凝集や損失が生じ、全体的な性能が低下する可能性があります。
ザルトリウスでは、Sartoclear®デプスフィルター、低結合フィルターを備えたTFF用Hydrosart®カセット、品質保証(QA)付きモノリシック技術など、不純物や空のカプシドを効率的に除去するソリューションをご提供しております。さらに、Recombumin®組換えヒトアルブミンはAAVの凝集を防止します。
関連ページ
AAV遺伝子治療に関するその他の製品、サービス、およびトレーニングをご覧ください。